Periyodik Tablo
Periyodik tablo özellikleri bakımından elementler iki büyük gruba (metaller, ametaller) ayrılır. Metaller ile ametalleri ayıran sınır bölgesinde her iki grubun özelliklerini taşıyan bazı elementler bulunur. Bu elementlere yarımetal ismi verilir.
Elementler tabloda A ve B grubu elementler olmak üzere ikiye ayrılırlar. A grubu elementleri baş grup elementler (s ve p), B grubu elementlerine de geçiş elementleri (d) ismi verilir. Geçiş elementleri, periyodik çizelgede IIA ile IIIA grubu elementleri arasında bulunurlar.
Çizelgedeki yatay sıralara periyot, düşey sıralara grup ismi verilir. Doğadaki element sayısı 89 tane olup, laboratuvarda sentetik yolla çekirdek reaksiyonları ile elde edilen ve radyoaktif olan 20 elementle birlikte yaklaşık 109'u bulmaktadırlar. Doğadaki 89 elementin oda sıcaklığında 15'i gaz, 2'si sıvı ve 72'si de katıdır.
Elementlerin isimlendirilmesi;
Çekirdek etrafında elektron bulutları ile sarılmış küresel bir hacim işgal eden nötral bir atomun çapını kesin olarak bulmak oldukça güçtür. Ancak elektron bulutunun belirli bir hacimde sınırını çizerek oluşturulan küre atomun şeklini belirler. Buna göre belirlenmiş atomun çapı periyodik tabloda periyodlarda yatay olarak ilerledikçe -atom numarası arttıkça- küçülür. Nedeni yatay olarak ilerledikçe atomun dış kabuğuna bir elektron ve çekirdeğe de bir proton eklenir. Ancak kabuğa eklenen bir elektronun atomun hacmini genişletme gücü, çekirdeğe katılan bir protonun atomun hacmini küçültme gücüne eşit değildir. Daha küçüktür. Protonun atomun hacmini küçültme gücü galip geldiğinden atom çapı yatay olarak gittikçe küçülür.
Atomik çaplar gruplarda aşağı doğru indikçe büyür. Çünkü her grupta elektron bir üst kabuğa girer (n=2, n=3,... gibi) ve ilave protonların atom çapını küçültme etkisi, üst kabuğa girmiş bulunan elektronların çapı büyültme etkisinin yanında küçük kalır. 5B'da n=2 kabuğu varken 13Al'de n=3 kabuğu vardır. 5B'un atomik çapı 0.080 nm, 13Al'mun ki ise 0.143 nm'dir. Bütün bunların yanında elektron kaybettiği zaman oluşan iyonun çapının daha küçük, elektron kazandığı zaman oluşan iyonun çapının da daha büyük olacağı bilinmektedir.
Atom büyüklüğü arttıkça iyonlaşma enerjisi azalır. Buna göre periyotlarda soldan sağa doğru gittikçe atom çapı küçülür ve iyonlaşma enerjisi artarken, gruplarda yukarıdan aşağı indikçe atom çapı büyüdüğünden iyonlaşma enerjisi azalır.
Bazı elementlerin I. iyonlaşma enerjileri (kJ/mol).

Elektron İlgisi:
İyonlaşma olayının tersine, gaz halindeki bir atomun bir elektron yakalaması ile açığa çıkan enerjiye elektron ilgisi denir. Bu durumda eksi yüklü bir iyon oluşur.
Atoma yaklaşan elektron atoma ait elektron bulutu tarafından itilirken çekirdek tarafından da çekilir. Bu çekme itmeden büyük olursa enerji yayınlanır. Birinci elektron alma çoğunlukla enerji yayınlar (ekzotermik) fakat ikinci ve üçüncü elektron almalar daima dışarıdan enerji isteye (endotermik) olaylardır.
Bazı elementlerin elektron ilgileri.
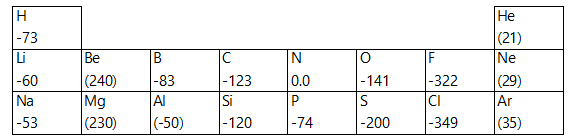
Elektronegatiftik:
Elektronegatiflik iyonlaşma enerjisi ve elektron ilgisini birleştiren bir tanımdır. Bir atomun molekül içinde bir kimyasal bağda elektronları kendine doğru çekme yeteneğidir. Elektronegatiflik periyodik tabloda soldan sağa gittikçe artar, yukarıdan aşağı indikçe azalır. Elektronegatifliği en yüksek olan flor için 4.0 standart kabul edilerek buna göre diğer bazı elementlerin elektronegatiflik değerleri ve elementlerin atom numaraları ile elektronegatiflik değerlerinin değişimi grafiği aşağıda verilmiştir.
İzoelektronik:
Bazı elementler elektron alıp vererek diğer bazı kementlerin elektron sayısına eşit elektrona sahip olabilirler. Elektron sayıları eşit olan element veya iyonlara izoelektronik ismi verilir. Örneğin 10Ne 10 elektron, 9F 9 elektrona sahiptir. Flor bir elektron daha alarak 10 elektrona sahip (F iyonu) olur. Böylece 10Ne ile 9F - izoelektroniktir denir. Buna benzer şekilde 7N3-, 8O2-, 9F-, 10Ne , 11Na+ , 12Mg2+, 13Al 3+ birbiriyle izoelektroniktir. Hepsinin on elektronu bulumaktadır.
Periyodik tablo özellikleri bakımından elementler iki büyük gruba (metaller, ametaller) ayrılır. Metaller ile ametalleri ayıran sınır bölgesinde her iki grubun özelliklerini taşıyan bazı elementler bulunur. Bu elementlere yarımetal ismi verilir.
Elementler tabloda A ve B grubu elementler olmak üzere ikiye ayrılırlar. A grubu elementleri baş grup elementler (s ve p), B grubu elementlerine de geçiş elementleri (d) ismi verilir. Geçiş elementleri, periyodik çizelgede IIA ile IIIA grubu elementleri arasında bulunurlar.
Çizelgedeki yatay sıralara periyot, düşey sıralara grup ismi verilir. Doğadaki element sayısı 89 tane olup, laboratuvarda sentetik yolla çekirdek reaksiyonları ile elde edilen ve radyoaktif olan 20 elementle birlikte yaklaşık 109'u bulmaktadırlar. Doğadaki 89 elementin oda sıcaklığında 15'i gaz, 2'si sıvı ve 72'si de katıdır.
Elementlerin isimlendirilmesi;
- O elementi keşfeden kişinin isminden yararlanarak (Küriyum, Einsteiniutn, Fermium gibi),
- Elementlerin keşfedildiği ülke veya şehrin ismine göre (Fransium, Germanyum, Polonyum,... gibi),
- Elementin özelliğine göre (hidrojen: nydro=su, genes=üreten) ve çoğunlukla latince kelimelerle yapılmıştır, helyum: helios=güneş, lithium: lithos=kaya, selen=ay gibi latince kelimelerden türetilmiştir.
Çekirdek etrafında elektron bulutları ile sarılmış küresel bir hacim işgal eden nötral bir atomun çapını kesin olarak bulmak oldukça güçtür. Ancak elektron bulutunun belirli bir hacimde sınırını çizerek oluşturulan küre atomun şeklini belirler. Buna göre belirlenmiş atomun çapı periyodik tabloda periyodlarda yatay olarak ilerledikçe -atom numarası arttıkça- küçülür. Nedeni yatay olarak ilerledikçe atomun dış kabuğuna bir elektron ve çekirdeğe de bir proton eklenir. Ancak kabuğa eklenen bir elektronun atomun hacmini genişletme gücü, çekirdeğe katılan bir protonun atomun hacmini küçültme gücüne eşit değildir. Daha küçüktür. Protonun atomun hacmini küçültme gücü galip geldiğinden atom çapı yatay olarak gittikçe küçülür.
Atomik çaplar gruplarda aşağı doğru indikçe büyür. Çünkü her grupta elektron bir üst kabuğa girer (n=2, n=3,... gibi) ve ilave protonların atom çapını küçültme etkisi, üst kabuğa girmiş bulunan elektronların çapı büyültme etkisinin yanında küçük kalır. 5B'da n=2 kabuğu varken 13Al'de n=3 kabuğu vardır. 5B'un atomik çapı 0.080 nm, 13Al'mun ki ise 0.143 nm'dir. Bütün bunların yanında elektron kaybettiği zaman oluşan iyonun çapının daha küçük, elektron kazandığı zaman oluşan iyonun çapının da daha büyük olacağı bilinmektedir.
İyonlaşma Enerjisi:
Herzaman dışarıdan ısı alan (endotermik) bir kimyasal olaydır. Gaz halindeki bir atomdan bir elektronu çıkarabilmek için gerekli minimum enerjiye iyonlaşmaenerjisiismi verilir. Bir elektronu çıkarmak için gerekli enerji birinci iyonlaşma enerjisi, ikinciyi çıkarmak için gerekli enerji ikinci iyonlaşma enerjisi üçüncüyüçıkarmak için gerekli enerjide üçüncü iyonlaşma enerjisi ismini alır. Tabii ki birinci iyonlaşmadan sonra + yüklü bir iyon oluşur. Artık bu + yüklü iyondan ikinci bir elektronu çıkarmak veya üçüncü bir elektronu çıkarmak daha büyük bir enerji gerektirir.Atom büyüklüğü arttıkça iyonlaşma enerjisi azalır. Buna göre periyotlarda soldan sağa doğru gittikçe atom çapı küçülür ve iyonlaşma enerjisi artarken, gruplarda yukarıdan aşağı indikçe atom çapı büyüdüğünden iyonlaşma enerjisi azalır.
Bazı elementlerin I. iyonlaşma enerjileri (kJ/mol).

Elektron İlgisi:
İyonlaşma olayının tersine, gaz halindeki bir atomun bir elektron yakalaması ile açığa çıkan enerjiye elektron ilgisi denir. Bu durumda eksi yüklü bir iyon oluşur.
Atoma yaklaşan elektron atoma ait elektron bulutu tarafından itilirken çekirdek tarafından da çekilir. Bu çekme itmeden büyük olursa enerji yayınlanır. Birinci elektron alma çoğunlukla enerji yayınlar (ekzotermik) fakat ikinci ve üçüncü elektron almalar daima dışarıdan enerji isteye (endotermik) olaylardır.
Bazı elementlerin elektron ilgileri.
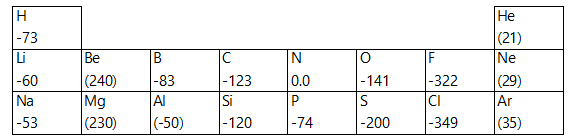
Elektronegatiftik:
Elektronegatiflik iyonlaşma enerjisi ve elektron ilgisini birleştiren bir tanımdır. Bir atomun molekül içinde bir kimyasal bağda elektronları kendine doğru çekme yeteneğidir. Elektronegatiflik periyodik tabloda soldan sağa gittikçe artar, yukarıdan aşağı indikçe azalır. Elektronegatifliği en yüksek olan flor için 4.0 standart kabul edilerek buna göre diğer bazı elementlerin elektronegatiflik değerleri ve elementlerin atom numaraları ile elektronegatiflik değerlerinin değişimi grafiği aşağıda verilmiştir.
İzoelektronik:
Bazı elementler elektron alıp vererek diğer bazı kementlerin elektron sayısına eşit elektrona sahip olabilirler. Elektron sayıları eşit olan element veya iyonlara izoelektronik ismi verilir. Örneğin 10Ne 10 elektron, 9F 9 elektrona sahiptir. Flor bir elektron daha alarak 10 elektrona sahip (F iyonu) olur. Böylece 10Ne ile 9F - izoelektroniktir denir. Buna benzer şekilde 7N3-, 8O2-, 9F-, 10Ne , 11Na+ , 12Mg2+, 13Al 3+ birbiriyle izoelektroniktir. Hepsinin on elektronu bulumaktadır.